最近科学家发现神秘的LINE1基因-一种人们长期认为是垃圾或有害寄生物的“跳跃基因”,实际上是胚胎发育初始阶段的一种关键的调节因子!说这个以前我们还是简单说说“跳跃基因”也称为“转座子”(transposon)的情况:
“跳跃基因”-会“跳舞”的基因
会“跳舞”的基因?非生物专业的童鞋们恐怕都会萌生好奇之心,想一探究竟,这是什么样的基因呢?为什么说它会“跳舞”呢?接下来,我们一起走进这种神奇基因的奥妙无穷的世界。
1983年,诺贝尔生理学或医学奖颁给了81岁的美国遗传学家巴巴拉.麦克林托克(Barbara McClintock),由此肯定她30多年前发现的基因跳跃现象(转座子),这是世界上靠独自研究成果获得此类奖金的第一位女科学家。这位被誉为“玉米夫人”的麦克林托克一生与玉米为伴,致力于玉米研究,首先发现玉米中有的单个基因是能跳跃的,即从染色体的一个位置跳到另一个位置,甚至从一条染色体跳到另一条染色体上。麦克林托克把这种会“跳舞”的基因称为“转座因子”,目前通称“转座子”(transposon)。从此,转座子走进人们的视野,受到越来越多的关注,成为科学家的宠儿。

美国遗传学家巴巴拉.麦克林托克
转座子是通过转录或逆转录方式,在内切酶的帮助下,能在生物染色体间移动的一段DNA序列。转座子的移动过程称为转座,转座可以发生在同一条染色体上,也可以发生在不同染色体间。转座子也称为转座因子、转座元件、转位子、可移动基因、跳跃基因。
那么,转座子是如何移动的呢?
目前,已知的转座子主要通过两种方式进行转座:复制型转座和非复制型转座。顾名思义,以复制型转座的转座子在转座时,会先将转座子DNA转录形成RNA中间产物,再逆转录形成新的相同的DNA,新形成的转座子DNA移动到其它新位置,而在原来位置仍保留有原来的转座子,即“复制和粘贴”的转座机制,这个过程需要转座酶和解离酶的参与;而以非复制型转座的转座子则直接从原来的位置切除下来并转移到新的位点,即“剪切和粘贴”的转座机制,这个过程不会形成RNA中间产物,只需要转座酶参与。转座酶和解离酶是转座子的亲密伙伴,转座酶既能像剪刀将DNA切断,又能如胶水将切下来的DNA粘贴到新的位点,转座酶作用于原来的转座子,而解离酶这种核酸内切酶则对新复制的转座子DNA起作用。
转座子的分类
转座子是一个非常庞大的家族,里面有很多家族成员,这些成员“风格迥异”,却又彼此有着不可分割的“血缘”关系。现在大概介绍下这些家庭成员,根据转座机制的不同,转座子可分为两大类:DNA转座子和逆转录转座子。DNA转座子仅占转座子的1%-2%,多采用“剪切和粘贴”的转座机制,而逆转录转座子所占比例高达86%,采用“复制和粘贴”的转座机制。逆转录转座子包括LTR转座子和不含LTR的转座子。LTR转座子又分成LINE(longinterspersed nuclear elements)我们下面要介绍的主角就属于这种,以及SINE(short interspersed nuclear elements),不含LTR的转座子由三个亚家族组成。那么LTR是什么呢?LTR(Long terminal repeat, LTR),即长末端重复序列,位于转座子的左右两端,由相同的DNA序列重复几百次甚至高达上千次形成,虽然LTR不能编码蛋白质,但它携带有转录起始和终止信号,以满足以RNA为中间产物的复制型转座的需要。
根据转座子的自主性,转座子又可分为自主型转座子和非自主型转座子。自主型转座子自身就能编码转座酶自主发生转座,而非自主型转座子必须在自主型转座子的帮助下才能够进行转座。日常生活中我们看到的玉米籽粒上的斑斑点点就是一个很好的佐证,麦克林托克发现这是由玉米的激活-解离系统(简称Ac/Ds系统)引起的,其中,Ac具有合成转座酶的功能,能自主进行移动,Ds则是非自主型转座子,要在Ac转座子存在时才能进行转座。这两种因子距离色素基因较近,如果Ac成功地帮助Ds插入到色素基因中,就会阻碍色素的合成,在籽粒上就会出现无色部分;如果Ds插入到隐性无色基因中,就会导致无色基因突变为有色基因,在籽粒上出现有色部分。
转座子广泛存在于生物细胞中,从简单的细菌到复杂的人类。转座子曾被误解为是“垃圾”DNA,但科学家们已为其辟谣,它们的作用也愈发凸显,如引起基因突变、促进生物进化、调节基因表达。研究表明,癌组织中也存在转座子活化现象,而且转座子的插入是与癌症发展同时发生的。另外,还有些转座子在胚胎发育早期和神经元中表达上调,比如神秘的LINE1基因,它构成人类17%基因,但目前科学家才开始逐渐了解它。
下面来介绍我们的明星“跳跃基因”-LINE1基因:
LINE1基因像其它转座因子(transposons)一样,拥有独特的复制功能,并且能随机插入基因组。当LINE1基因插入较坏的基因组位置,遗传学家通常会更关注它,因为这潜在导致癌症或者血友病(hemophilia)等遗传疾病。如果该基因插入良性基因组位置,就无害;如果该基因插入恶性基因组位置,就有害。来自加州大学旧金山分校发展生物学家米盖尔·玛尔霍·桑托斯(Miguel Ramalho-Santos)认为LINE1基因值得深入研究,他个人认为这是一种不同寻常的DNA片段。它在人类基因中重复50多万次,几乎占每个细胞的五分之一。那为什么它会在人类基因组中保持如此多的数量呢?
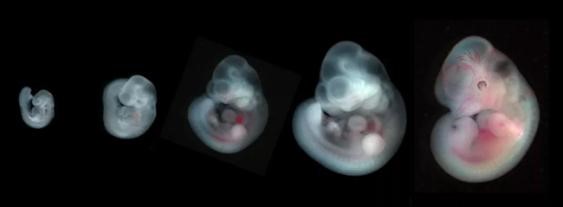
在小鼠胚胎早期发育过程中,胚胎干细胞会大量表达LINE1。从常规角度来看,真是不知道胚胎在想啥,表达这么多转座子,是嫌还不够天下大乱吗?但是仔细一观察,表达出的RNA都聚集在细胞核附近,显然是在我们不知道的地方发生了些什么。
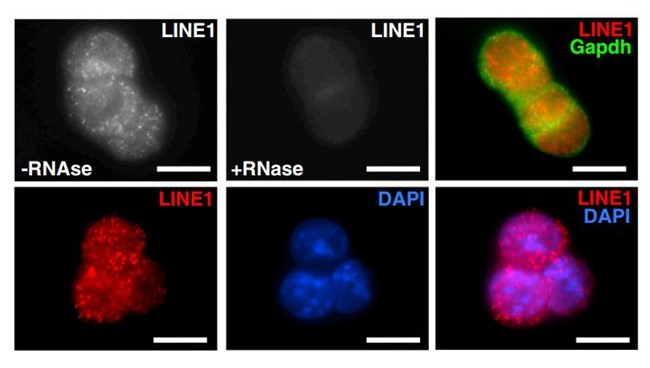
LINE1表达集中在细胞核
桑托斯和其他同事发现LINE1基因在胚胎发展过程中尤为活跃,这表明该基因片段在协调胚胎细胞发育过程中发挥着重要作用。他开始做一些实验,直到米歇尔·珀查德(Michelle Percharde)以博士后身份加入实验室团队,桑托斯才找到一个真实承担LINE1基因研究的合作伙伴,桑托斯的实验取得了进展,LINE1基因研究逐渐步入正轨,他们着手尝试清除LINE1。直接敲除是不可能的了,毕竟LINE1占据基因组近1/5,都敲掉DNA怕不是要碎成沫沫。于是研究者开发了一套利用寡义核苷酸敲低RNA的方法,将细胞内LINE1RNA的水平降低到了正常的水平的80-90%。
万万没想到啊,这一敲低可坏了大事了,胚胎干细胞的自我更新能力几乎就是没了,不会分裂了;更吓人的是,如果在胚胎发育过程中进行敲低,那么受精卵分裂成两个细胞之后,整个发育过程就再也走不下去了,几乎没有谁能够突破这个难关长到四细胞阶段,更别提长成一个真生命了!
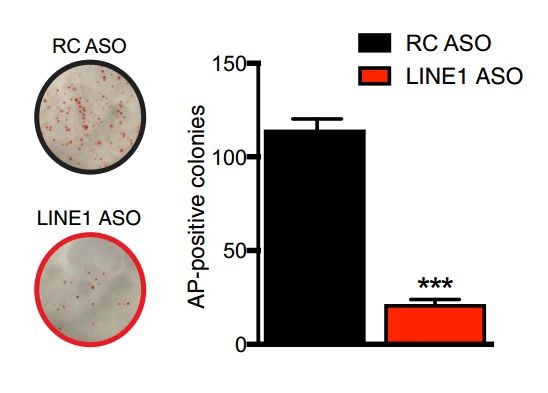
敲低LINE1之后胚胎干细胞自我更新能力几乎没了
原来LINE1RNA真的没有闲着,它在细胞核内会与两种重要的蛋白握手——一种叫做核蛋白,它是核糖体的组成部分;另一种稍微陌生一些,叫做Kap1,这种蛋白能够与多种转录因子集合,具有关键的转录调控作用。LINE1RNA与它俩形成的复合体才是LINE1作用的完全体,它们接下来完成了两项重大任务。这组复合体能够抑制一个名为Dux的基因表达。Dux就是一个转录因子了,它和两细胞阶段很多必须的基因都关系匪浅。这些基因是胚胎发育两细胞阶段必须的,但是一个阶段有一个阶段的任务,想要继续发育,就必须让它们歇歇了。转录组分析也显示,Dux靶向的那些基因,正是敲低LINE1之后最活跃的那些。与此同时,LINE1RNA复合体还有一个重要的工作,就是激活rRNA的表达。不用多解释了,rRNA是组成核糖体必须的,也是细胞翻译蛋白所必须的。这就是为啥敲低了LINE1之后胚胎干细胞自我更新能力降低的原因。
有趣的是,LINE1在发育中的重要功能,和它“转座”的本性似乎并不相关。研究者尝试着阻止LINE1的逆转录,胚胎干细胞的发育也很正常。研究者猜想,胚胎细胞可能自有一套调教LINE1的方法,让它的RNA在出工出力的同时,又不会瞎跳跃给基因组造成太大的麻烦。
在过去几年里,其他研究小组曾偶然间发现LINE1基因功能的重要线索。他们发现LINE1基因在早期老鼠胚胎和大脑细胞中可能发挥的作用,但是他们并没有对LINE1基因功能提供确凿证据。美国南达科达州立大学LINE1基因研究员Wenfeng An说:“直到近期,关于LINE1基因的探索仍没有准确的定论,我们一直在期望着研究结果,这是一项开创性研究。”
科学家下一步将重点研究人类细胞中的LINE1基因,它构成人类基因的17%。老鼠和人类存在着差异,但是LINE1基因也大量存在于差不多所有的哺乳动物。研究者下一步就准备分析是否人类也存在类似的机制。虽然小鼠和人的差距很大,但是要知道,LINE1几乎是人类基因组中唯一的还十分活跃的转座子,同时也含量巨大,真的很难不让人认为进化之手故意留下它是别有用心呢。其他的转座子(也被认为是垃圾DNA)在人类细胞发育过程中也具有重要作用。美国斯坦福大学发展生物学家乔安娜·沃索西卡(Joanna Wysocka)之前也研究过LINE1基因,她说:“在所谓的垃圾基因中存在大量的‘宝藏’。


